距离2023年北京各区高中期末考试还有不到一个月的时间,为了更好的帮助备考复习,查缺补漏。北京高考在线为大家整理了2024高考化学铁离子和亚铁离子的检验方法!希望对大家高中化学答题及备考有帮助!
2024高考化学铁离子和亚铁离子的检验方法
【要点解读】
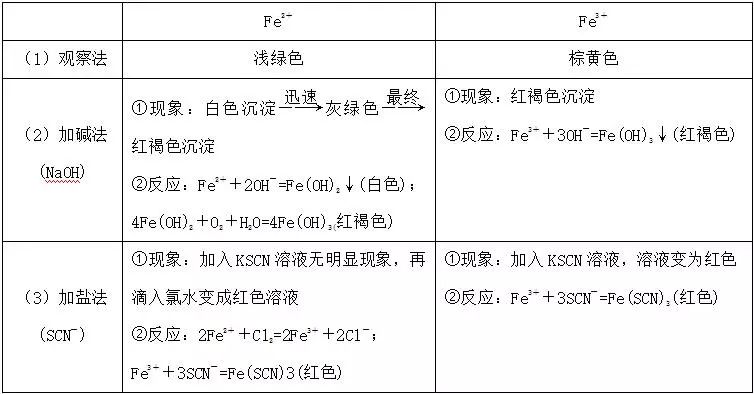
特别提醒 检验Fe2+的注意事项
(1)只含Fe2+的溶液:检验Fe2+加入试剂的顺序

①加KSCN溶液前,防止加入氧化性的物质,使Fe2+氧化。
②氧化剂不能选用酸性KMnO4溶液,原因:酸性KMnO4溶液本身显紫红色,对Fe(SCN)3红色有干扰;酸性KMnO4溶液能氧化KSCN,溶液不变红色,不能证明不含Fe2+。
(2)同时含有Fe2+和Fe3+的溶液
Fe2+对检验Fe3+无干扰,可以滴加KSCN溶液检验Fe3+;Fe3+对检验Fe2+有干扰,不能采用加KSCN溶液检验Fe2+,通常向溶液中滴加适量酸性KMnO4溶液,溶液紫红色褪色说明含有Fe2+。
(3)检验铁的氧化物中是否有+2价铁时,正确的思路为

①步骤a中不能选用盐酸,原因是酸性KMnO4溶液可以氧化盐酸。
②步骤a中,不能选用稀HNO3,原因是稀HNO3可以将Fe2+氧化为Fe3+。
【名师点睛】注意亚铁离子与铁离子性质的区别,检验时必须有明显不同的现象,要排除Fe3+的干扰,
利用两离子的性质差异,即亚铁离子具有还原性,可与氯水、高锰酸钾等氧化剂反应,以此解答该题。
【重难点点睛】通常检验三价铁离子的检验方法有:取待测液于试管中,向待测溶液中加入KSCN溶液,
溶液马上变成红色说明溶液中有Fe3+,即Fe3++3SCN-=Fe(SCN)3;也可以所以苯酚,铁离子与苯酚发生颜色反应;还可以根据与碱溶液生成红褐色沉淀,判断溶液中存在铁离子。
【名师点睛】先根据Fe3+的特征反应判断溶液不含Fe3+;然后加入氧化剂,如果含有Fe2+,Fe2+被氧化剂氧化成Fe3+溶液变成红色,以此证明Fe2+的存在。
声明:本文由北京高考在线团队(微信公众号:bjgkzx)排版编辑,内容来源于网络,如有侵权,请及时联系管理员删除。




































